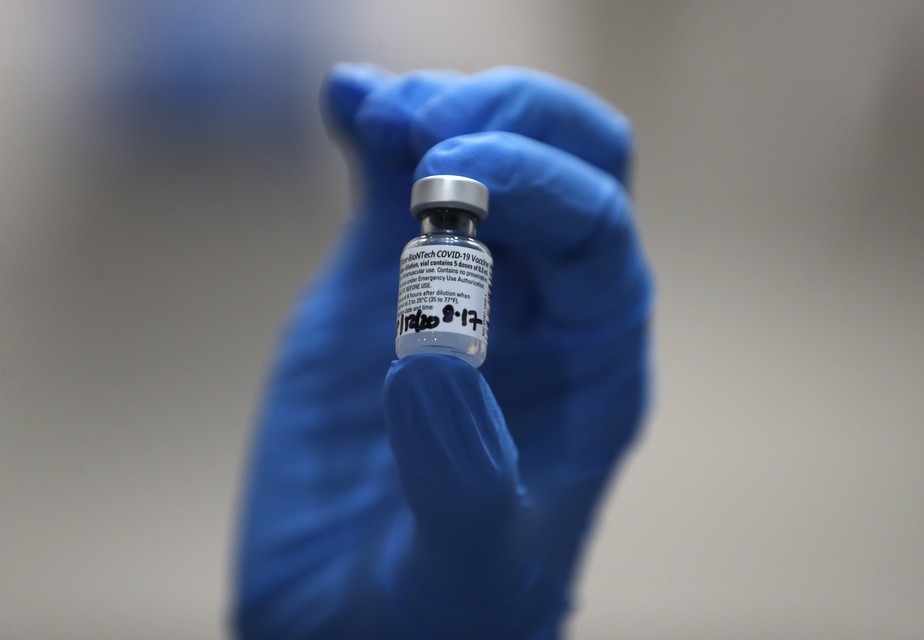
A área técnica da Agência Nacional de Vigilância Sanitária (Anvisa) autorizou nesta quinta-feira (16) a aplicação da vacina da Pfizer contra Covid-19 em crianças de 5 a 11 anos. A dosagem para esse público será menor do que a utilizada por maiores de 12 anos. O Brasil ainda não tem essas doses ajustadas.
A Anvisa alerta que a autorização é baseada nos dados disponíveis até o momento e os resultados são avaliados a todo momento.
Para o infectologista Renato Kfouri, representante da Sociedade Brasileira de Imunizações e que participou da avaliação da Pfizer junto à Anvisa, vacinar essa faixa etária é importante para a redução do número de casos graves e mortes causadas pela doença nessa faixa etária.
“A gente fala que só 0,4% das mortes ocorrem nos menores de 20 anos, mas 0,4% de 600 mil mortes são mais de 2.500 crianças e adolescentes que perderam a vida para a Covid. Em dois anos, esse total de mortes é maior do que todo o calendário infantil. Se somarmos todas as mortes por coqueluche, diarreia, sarampo, gripe, meningite, elas não somam 1.500 por ano. A Covid-19 é uma doença prevenível por vacina que mais mata nossas crianças”, diz.
Ele reforça que existem justificativas sanitárias, epidemiológicas, de saúde pública para incluir crianças no programa de imunizações. “Claro, desde que as vacinas sejam seguras, com o mesmo critério e rigor que licenciamos para os adultos. Cumprindo esses critérios, não há dúvidas que é importante vacinar essa faixa etária”, completa.
O pedido para ampliação do uso da vacina da Pfizer para essa faixa etária havia sido apresentado em 12 de novembro. A farmacêutica informou que a dosagem para essa faixa etária será menor. Além disso, os frascos terão a tampa da cor laranja, para diferenciar das doses já usadas em maiores de 12 anos.
"A redução na dosagem para a faixa de 5 a 11 anos se respaldou nos estudos de Fase 1 e 2, que mostraram que essa dosagem (10 microgramas) foi o suficiente para gerar altos títulos de anticorpos com perfil de segurança bastante favorável para a população pediátrica", informou a Pfizer.
A avaliação levou 21 dias, descontados os 14 dias que a Pfizer utilizou para responder exigências técnicas da Anvisa. O tempo total do processo na agência foi de 35 dias.
G1












0 comentários